後発医薬品の製造メーカーの小林化工が2020年に同社が製造した爪水虫などの治療薬イトラコナゾール錠50「MEEK」に睡眠導入剤成分が混入した問題を起こしました。
その報告書が提出されましたが製薬業界関係者以外であればこの報告書を読むことは大変難しいです。
[box06 title=”あわせて読みたい”]睡眠導入剤混入の小林化工、事故調査結果報告書5つのポイントを解説 [/box06]今回の記事では医薬業界に勤める筆者が報告書の中で使われている用語の中で大切な用語だけをピックアップし解説していきます。
報告書を少し読んでみたけど内容が全く分からないという方はこの記事でキーワードを押さえてから報告書を読んでみて下さい。
[box06 title=”あわせて読みたい”]睡眠導入剤混入の小林化工、事故調査結果報告書5つのポイントを解説小林化工と日医工の社員はどうなるのか? |過去の不正事例から考える|
小林化工の問題点を製薬製造現場を知る技術者が考える 品質管理部門編
小林化工の問題点を製薬製造現場を知る技術者が考える GMP編
[/box06]GMP省令とは薬の製造・販売ルール
GMPとはGood Manufacturing Practiceの略で薬の製造業者と販売業者に求められる製造管理・品質管理基準の事です。
GMP省令は厚生労働が定めた省令で「医薬品及び医薬部外品の製造管理及び品質管理の基準」に関する省令です。
薬を消費者に安全に届けるために「誰がいつ作業しても必ず同じ品質・高い品質の製品を作るために、行うべきこと」と厚生労働省によって作られたルールです。
GMP違反をすると県から業務改善命令や業務停止命令を受けます。
小林化工は事故調査報告書の結果、多数のGMP違反が確認されました。
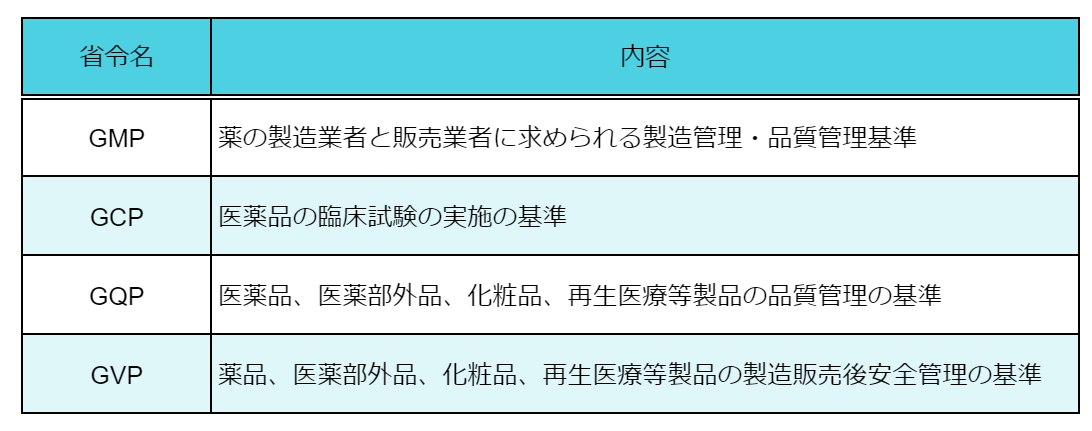
GCP省令とGQP省令とGVP省令の違い
GCPとは(Good Clinical Practice)の略で医薬品の臨床試験の実施の基準に関する省令です。
「くすりの候補」の人における効果(有効性)と安全性を調べる治験は、科学的な方法で、参加される方の人権を最優先にするためのルールです。
GQPとはGood Quality Practiceの略で医薬品、医薬部外品、化粧品、再生医療等製品の品質管理の基準に関する省令です。
また薬の製造販売業者は品質保証責任者を設置する事をGQPでは定めています。
GVPはGood Vigilance Practiceの略で医薬品、医薬部外品、化粧品、再生医療等製品の製造販売後安全管理の基準に関する省令です。
副作用や感染症を対象とした、薬の販売後のトラブルに対して製造や品質の改善や日々の情報収集を行いなさいと言っているルールです。
医薬品と医薬部外品
医療用医薬品とは医師の診断のもと医師が処方箋をだして薬剤師が調剤する医薬品です。
一般用医薬品とは医師の処方箋なしに薬局やドラックストアで購入することができる医薬品です。
また医薬部外品と呼ばれる薬もあります。
医薬部外品は、医薬品に似ているが作用が緩和なもので治療目的よりは予防・衛生目的で作られています。
小林化工は主に医療用医薬品を製造しています。
PMDAは医薬品を審査している独立行政法人
PMDAとは独立行政法人医薬品医療機器総合機構「Pharmaceuticals and Medical Devices Agency」の略です。
厚生労働省所管の独立行政法人で以下の業務を行っています。
・医機法に基づく医薬品・医療機器などの審査関連業務
・医薬品の副作用などによる健康被害救済業務
・医薬品や医療機器などの安全性を確保する安全対策業務及び情報提供業務(審査報告書、添付文書情報等提供)
医薬品の製造販売承認を受けるためには、製造体制がGMPに適合していることが確認する必要がありますがその確認をPMDA又は都道府県が行っています。
小林化工のGMP適合確認は都道府県(福井県)が担当していました。
ジェネリック医薬品と先発医薬品の違い
「ジェネリック医薬品(後発医薬品)」は、「新薬(先発医薬品)」の特許が切れたあとに販売される薬です。
新薬と同じ有効成分・品質・効き目・安全性が同等であると国から認められています。
新薬に比べ開発費が抑えられるために低価格で消費者に届けることができます。
先発メーカーにはこのような会社があります。
- 塩野義製薬
- 武田薬品
- エーザイ
ジェネリックメーカーには
- 沢井製薬
- 日医工
- 東和薬品
これらの会社が有名です。
小林化工もジェネリックメーカーの1つです。
薬機法とは医薬品に関する法律
薬機法とは、正式名称を「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」といいます。
この名称は2014年(平成26年)11月から使われています。
それ以前は薬事法という名称でした。
小林化工がジェネリックメーカーとして急成長できた要因の一つが2002年の薬事法改正でした。
2002年の薬事法改正では製造販売業という概念が創設され、自らが製造販売する医薬品の製造を外部委託することができるようになりました。
これにより小林化工は大手製薬会社からの受託製造を拡大し医療用医薬品の販売実績を拡大させることに成功しました。
SOPとは標準作業手順書である
SOPとは、Standard Operating Proceduresの略で、日本語では「標準作業手順書」といいます。
医薬品製造業界では当たり前に使われている言葉で医薬品を作るための手順書です。
医薬品製造業者はGMP省令に基づきSOPを作成しなければいけません。
医薬品の製造過程では作業者がSOPに従い作業をすることにより均一で安全な薬を製造することができます。
小林化工ではSOP上、記載されている工場とは別の工場で一部の薬が作られていたことが分かっており、これはSOP違反でありGMP違反です。
製造販売業者に対する三役制度
GQPやGVPを遵守するめに薬機法では製造販売業者に対して3つの責任者を置くことを課しています。
- 安全管理責任者(GVP)
- 品質保証責任者(GQP)
- 統括製造販売責任者
小林化工ではこれら三役に加えて代表取締役社長、製造管理者、営業本部長、渉外事業本部長が毎月集まり、他社販売を含めた回収事例や品質情報、逸脱、安全性情報を共有し対策を検討しています。
2020年1月からは会議の名称が「製販三役連絡会議」となっています。
[box06 title=”あわせて読みたい”]睡眠導入剤混入の小林化工、事故調査結果報告書5つのポイントを解説小林化工と日医工の社員はどうなるのか? |過去の不正事例から考える|
[/box06]


の対応方法-300x158.png)





